Ультрафіолетова (UV-Vis) спектроскопія
- Огляд Джерело: Лабораторія д-ра Б. Джилла Вентона - Університету Вірджинії Ультрафіолетова (UV-Vis)...
- Процедура
- Результати
- Програми та резюме
Огляд
Джерело: Лабораторія д-ра Б. Джилла Вентона - Університету Вірджинії
Ультрафіолетова (UV-Vis) спектроскопія є однією з найпопулярніших аналітичних методів, оскільки вона дуже універсальна і здатна виявляти майже кожну молекулу. За допомогою УФ-візової спектроскопії світло УФ-Віс пропускають через зразок і вимірюють пропускання світла зразком. З коефіцієнта пропускання (T) поглинання можна розрахувати як A = -log (T). Отримано спектр абсорбції, який показує поглинання сполуки на різних довжинах хвиль. Величина абсорбції при будь-якій довжині хвилі обумовлена хімічною структурою молекули.
UV-Vis може бути використаний якісно, для ідентифікації функціональних груп або підтвердження ідентичності сполуки шляхом зіставлення спектру абсорбції. Він також може бути використаний кількісно, оскільки концентрація аналіту пов'язана з абсорбцією з використанням закону Біра. UV-Vis спектроскопія використовується для кількісної оцінки кількості ДНК або білка в зразку, для аналізу води, і як детектор для багатьох типів хроматографії. Кінетику хімічних реакцій вимірюють також ультрафіолетовою спектроскопією, приймаючи повторні вимірювання УФ-Vis за час. Вимірювання UV-Vis зазвичай приймають за допомогою спектрофотометра. UV-Vis також є дуже популярним детектором для інших аналітичних методів, таких як хроматографія, оскільки він може виявляти багато сполук.
Як правило, УФ-Віс не є найбільш чутливою технікою спектроскопії, оскільки не дуже багато світла поглинається на короткий шлях. Інші методи спектроскопії, такі як флуоресценція, мають більш високу чутливість, але вони не є такими загальноприйнятими, оскільки більшість молекул не є флуоресцентними. UV-Vis має подібну чутливість до інших вимірів абсорбції, таких як інфрачервона спектроскопія.
База даних JoVE Science Education. Аналітична хімія. Ультрафіолетова (UV-Vis) спектроскопія. JoVE, Cambridge, MA, (2019).
Принципи
UV-Vis часто називають загальною технікою, оскільки більшість молекул поглинають в діапазоні довжин хвиль UV-Vis. УФ випромінюється від 100 до 400 нм і видимий спектр від 400 до 700 нм. Діапазон 100–200 нм називається глибоким УФ. Джерела світла більш важко знайти для цього діапазону, тому він не використовується регулярно для вимірювань UV-Vis. Типові UV-Vis спектрометри використовують дейтерієву лампу для ультрафіолетового випромінювання, що виробляє світло від 170–375 нм і лампу вольфрамової нитки для видимого світла, яка виробляє світло від 350-2500 нм.
Коли фотон потрапляє в молекулу і поглинається, молекула просувається в більш збуджений енергетичний стан. УФ-видиме світло має достатньо енергії для просування електронів у вищий електронний стан, від найвищої зайнятої молекулярної орбіталі (HOMO) до найнижчої незайнятої молекулярної орбіталі (LUMO). Різниця енергії між HOMO і LUMO називається забороненою зоною. Як правило, ці орбіталі називаються склеювання і анти-склеювання. Енергія фотона повинна точно збігатися з забороненою зоною для фотону, що поглинається. Таким чином, молекули з різними хімічними структурами мають різні смуги енергетичних смуг і різні спектри поглинання. Найбільш поширеними переходами, які потрапляють в діапазон UV-Vis, є π-π * і n-π *. Pi-орбіталі виникають внаслідок подвійних зв'язків, а n-орбіталі - для незв'язувальних електронів. Pi зірка є анти-склеюючими пірбіталями. Таким чином, найкраще поглинання УФ-вісом відбувається молекулами, які містять подвійні зв'язки. Пі орбіталі, що примикають один до одного, пов'язані між собою, називають кон'югацією, зазвичай збільшує поглинання. Переходи Sigma-σ *, пов'язані з одинарними зв'язками, є більш високою енергією і потрапляють у глибоку УФ, тому вони менш корисні для рутинного використання. Поява широких смуг або плечей на структурі УФ-Віс обумовлена численними коливальними і обертальними станами молекули, які призводять до розділення енергетичних смуг енергії.
Для молекул з абсорбцією у видимій області сполуки часто будуть кольоровими. Тим не менш, поширеним помилкою є те, що довжина хвилі пікового поглинання (λmax) для сполуки є кольором, який він проявляє. З'єднання, яке виглядає червоним, не має великого поглинання в червоній області спектру. Замість цього λmax для сполуки, що виглядає червоною, є зеленим. Колір сполуки виникає тому, що ці довжини хвиль світла селективно передаються через зразок і, таким чином, вони не абсорбуються. Колірне коло є корисним при визначенні того, який колір буде поглинати сполука і в якому діапазоні буде λmax, оскільки колір безпосередньо через колесо від спостережуваного кольору - це колір, який найбільш поглинається.
Поглинання слід за законом Беера, A = εbC, де ε - молярний коефіцієнт ослаблення, b - довжина шляху, а C - концентрація. Молярний коефіцієнт ослаблення є характеристикою окремої сполуки для поглинання при даній довжині хвилі, і ця властивість обумовлена функціональними групами, кон'югацією тощо. Якщо з'єднання не має високого коефіцієнта ослаблення, воно може бути позначене відповідною групою збільшують його абсорбцію. Довжина шляху, як правило, пов'язана з розміром кювети і становить 1 см у стандартних спектрофотометрах.
UV-Vis виконується на різних інструментах, від традиційних спектрофотометрів до більш сучасних пристроїв для зчитування пластин. Довжину хвилі абсорбції слід вибирати, використовуючи фільтр або монохроматор. Монохроматор - це пристрій, який просторово розділяє довжини хвиль світла, а потім розміщує вихідну щілину, де потрібна довжина хвилі світла. Монохроматори можна сканувати, щоб забезпечити весь спектр абсорбції. Альтернативно, прилад з діодним масивом дозволяє всім кольорам світла передаватися через зразок, тоді світло розділяється на різні довжини хвиль просторово і виявляється за допомогою фотодіодів. Інструменти діодного масиву швидше збирають повні спектри, але є більш складними і дорожчими.
Процедура
1. Калібруйте спектрометр
- Увімкніть UV-Vis спектрометр і дайте лампам прогрітися протягом відповідного періоду часу (близько 20 хв), щоб стабілізувати їх.
- Наповніть кювету розчинником для зразка та переконайтеся, що зовні чиста. Це буде служити заготовкою і допомагає врахувати втрати світла внаслідок розсіювання або поглинання розчинником.
- Помістіть кювету в спектрометр. Переконайтеся, що кювету вирівняно належним чином, оскільки часто кювета має дві сторони, які призначені для обробки (можуть бути рифлені) і не призначені для освітлення світла.
- Зробіть читання для порожнього. Абсорбція повинна бути мінімальною, але будь-яку абсорбцію слід відняти з майбутніх зразків. Деякі інструменти можуть зберігати порожні дані і автоматично виконувати віднімання.
2. Виконайте спектр поглинання
- Наповніть кювету зразком. Щоб переконатися, що перенесення є кількісним, двічі промийте кювету зразком, а потім заповніть його близько ¾ повної. Переконайтеся, що зовні чисті відбитки пальців і т.д.
- Помістіть кювету в спектрометрі в правильному напрямку.
- Накрийте кювету, щоб запобігти впливу навколишнього світла.
- Збирають спектр поглинання, дозволяючи приладу сканувати через різні довжини хвиль і збирати поглинання. Діапазон довжин хвиль може бути встановлений з інформацією про конкретний зразок, але діапазон 200–800 нм є стандартним. Діодний масив може збирати весь спектр поглинання за один прогон.
- З зібраного спектру абсорбції визначають максимум поглинання (λmax). Повторіть збірку спектрів, щоб отримати оцінку похибки в λmax.
- Щоб скласти калібрувальну криву, збирайте спектр УФ-Віс різних зразків концентрації. Спектрометри часто обмежені в лінійному діапазоні і не можуть вимірювати величину поглинання більше 1,5. Якщо значення абсорбції для зразка знаходяться поза лінійного діапазону приладу, розбавляйте зразок, щоб отримати значення в межах лінійного діапазону.
3. Кінетичні експерименти з УФ-спектроскопією
- UV-Vis може бути використаний для експериментів з кінетики шляхом вивчення зміни абсорбції з плином часу. Для експерименту з кінетикою беруть початкове зчитування зразка.
- Швидко додайте реагент для початку хімічної реакції.
- Добре перемішують, щоб змішатися з зразком. Якщо додати невелику кількість, це можна зробити в кюветі. Альтернативно, змішати реагент з зразком і швидко влити в кювету для вимірювання.
- Вимірюють поглинання при λmax для аналіту, що представляє інтерес, протягом часу. Якщо використання реагенту вимірюється ( тобто поглинання зростає, тому що реагент менше абсорбується), то розпад покаже порядок реакції.
- Використовуючи калібрувальну криву, зробіть графік концентрації аналіту проти часу, перетворюючи значення абсорбції в концентрацію. Звідси цей графік може бути придатним до відповідних рівнянь для визначення констант швидкості реакції.
Ультрафіолетові видимі, або UV-Vis, спектроскопія є однією з найбільш популярних аналітичних методів в лабораторії.
У УФ-Vis спектроскопії світло пропускається через зразок при певній довжині хвилі в УФ або видимому спектрі. Якщо зразок поглинає частину світла, не весь світ буде проходити або передаватися. Передача - це відношення інтенсивності прохідного світла до падаючого світла і корелює з поглинанням. Абсорбцію можна використовувати кількісно, щоб отримати концентрацію зразка. Він також може бути використаний якісно, щоб ідентифікувати з'єднання шляхом зіставлення виміряної поглинання в діапазоні довжин хвиль, званих спектром абсорбції, з опублікованими даними. Це відео введе спектроскопію УФ-ВІС і продемонструє його використання в лабораторії при визначенні концентрації зразків і кінетики реакції.
Коли фотон потрапляє в молекулу і поглинається, молекула просувається з її основного стану в більш високий енергетичний стан. Різниця енергії між цими двома полями є зазором. Для того, щоб фотон поглинався, енергія фотона повинна точно збігатися з забороненою зоною. Хімічна структура визначає ширину забороненої зони; тому кожна молекула має унікальні спектри абсорбції.
Абсорбція слідує Закону Беера, що свідчить про абсорбцію, що дорівнює коефіцієнту молярного ослаблення, що перевищує довжину шляху та концентрацію. Коефіцієнт молярного ослаблення пов'язаний зі здатністю окремої сполуки поглинати світло певної довжини хвилі. Довжина шляху відноситься до відстані, пройденої світлом через зразок, що зазвичай становить 1 см для стандартних кювет. Закон Біра можна використовувати для розрахунку концентрації зразка, якщо відома абсорбція, або може бути використана калібрувальна крива.
UV-Vis часто називають загальною технікою, оскільки більшість молекул поглинають світло в діапазоні довжини хвилі, що видно з УФ. УФ-спектр простягається від 100–400 нм, а видимий спектр - від 400 до 700 нм. Однак більшість спектрофотометрів не працюють у глибині УФ-діапазону 100–200 нм, оскільки джерела світла в цьому діапазоні коштують дорого. Більшість UV-Vis спектрофотометрів використовують дейтерієву лампу для УФ-діапазону, яка виробляє світло від 170–375 нм, і лампу вольфрамової нитки для видимого діапазону, яка виробляє світло від 350-2500 нм.
Оскільки джерело світла зазвичай є лампою з широкими діапазонами довжин хвиль, то специфічна довжина хвилі абсорбції вибирається за допомогою фільтрів або монохроматора. Монохроматор - це пристрій, який просторово розділяє довжини хвиль світла, а потім розміщує вихідну щілину, де потрібна довжина хвилі світла. Монохроматор можна сканувати в діапазоні довжин хвиль, щоб забезпечити весь спектр поглинання. Це робить техніку корисною для кількісного визначення та ідентифікації широкого спектру молекул.
Тепер, коли були викладені основи УФ-Vis спектроскопії, давайте розглянемо простий ультрафіолетовий експеримент у лабораторії.
Перш ніж почати вимірювання, ввімкніть спектрофотометр і дайте лампам прогрітися протягом відповідного періоду часу, щоб стабілізувати їх.
Приготуйте заготовку, заповнивши чисту кювету розчинником зразка, а потім протріть її зовні безворсовою папером, щоб видалити відбитки пальців.
Переконайтеся, що кювети вирівняні належним чином з будь-якою виїмкою зі сторони пучка, і вставте її в спектрофотометр. Закріпіть кришку, щоб запобігти потрапленню навколишнього світла в систему.
Вимірюють поглинання заготовки на одній довжині хвилі або в діапазоні довжин хвиль. Записують або зберігають абсорбцію, так як вона повинна відніматися від поглинання зразка.
Далі відкидають заготовку і двічі промивають кювету зразком. Потім заповнюють кювету близько ¾ повної зразка. Знову протріть кювету, щоб переконатися, що вона чиста і без відбитків пальців.
Помістіть кювету в спектрофотометрі в правильній орієнтації і зафіксуйте кришку.
Збирають вимірювання поглинання або спектр на тій же довжині хвилі або діапазоні довжин хвиль, що і заготовка. Відніміть порожній спектр або вимірювання, якщо прилад не робить це автоматично.
З зібраного спектру абсорбції визначають максимум поглинання, або λmax.
Для кількісної оцінки кількості аналіту в зразку створюють калібрувальну криву, використовуючи діапазон відомих концентрацій аналіту. Для отримання додаткової інформації про те, як побудувати та використати калібрувальну криву, перегляньте відео з цієї колекції "Криві калібрування".
Вимірювання поглинання можна також використовувати для розрахунку кінетики реакції шляхом вимірювання збільшення або зменшення концентрації сполук протягом усього процесу. Починають з початкового зчитування зразка, синього барвника в цьому випадку, на максимумі абсорбції перед реакцією.
Далі швидко додають реагент, відбілювач в цьому випадку, щоб почати хімічну реакцію. Добре перемішайте, щоб він змішувався з зразком.
Вимірюють абсорбцію на максимумі поглинання протягом часу.
Показано початковий спектр абсорбції зразка синього барвника. Кольори тла показують кольори світла у видимому спектрі. Синій барвник має максимум поглинання близько 630 нм.
Кінетику реакції між синім барвником і відбілювачем вимірювали протягом часу. Абсорбція синього барвника з часом зменшується, оскільки вона реагує з відбілювачем. Абсорбція досягає близько нуля через 300 с, що вказує на те, що реакція наближається до завершення. Для отримання додаткової інформації про кінетику та реакції, будь ласка, дивіться відео JoVE Science Education "Закони про швидкість реакції".
UV-Vis спектроскопія використовується в багатьох різних областях досліджень для ідентифікації або кількісної оцінки зразка.
Наприклад, УФ-Vis спектроскопія використовується в значній мірі в біологічних полях для кількісної оцінки кількості білка в зразку. Бредфорд-аналіз часто використовується для кількісного визначення білків за допомогою барвника. Спочатку готують калібрувальну криву відомих концентрацій білка, зазвичай з використанням альбуміну бичачої сироватки або BSA. Потім до кожної зі стандартів і до зразка додають Кумасси синю забарвлення. Потім поглинання комплексу білок-барвник вимірюють при 595 нм.
Альтернативно, білки можуть бути виміряні безпосередньо за їх абсорбції при 280 нм. У цьому прикладі концентрацію білка визначають кількісно, використовуючи спектрофотометр ультранизького об'єму. Для багатьох білків абсорбція 1 корелює з концентрацією 1 мг / мл.
Ультрафіолетова спектроскопія також використовується для кількісної оцінки кількості бактеріальних клітин в культурі клітин. Для цього вимірювання поглинання або оптична щільність вимірюють при 600 нм. Як правило, вимірювання OD600 1 вказує на присутність 8 × 108 бактеріальних клітин на мл. Вимірювання щільності клітин протягом росту культури дозволяє визначити криву бактеріального росту і може допомогти визначити, коли культура знаходиться в експонентній фазі росту.
Оксид азоту та діоксид азоту, або NOx, є побічним продуктом вихлопу автомобіля і може бути шкідливим для навколишнього середовища, оскільки він утворює пошкоджуючий тропосферний озон. NOx можна виміряти шляхом взаємодії його з розчином сульфаниловой кислоти і нафтилэтилендиамина. Отриманий розчин являє собою молекулу азо-барвника рожевого кольору, інтенсивність якої прямо корелює з концентрацією NOx. Цю концентрацію можна потім визначити, використовуючи спектрофотометр UV-Vis.
Ви тільки що спостерігали за введенням JoVE в УФ-видиму спектроскопію. Тепер ви повинні зрозуміти основи роботи UV-Vis, як виміряти зразок, використовуючи UV-Vis, і як співвідносити абсорбцію з концентрацією зразка.
Дякую за перегляд!
Результати
UV-Vis може бути використаний для отримання спектру кольорових сполук. На Фігурі 1А показаний спектр абсорбції синього барвника. Фон показує кольори світла у видимому спектрі. Синій барвник має абсорбцію λmax у помаранчевому / червоному кольорі. Рисунок 1B показує спектр червоного барвника, з λmax в зеленому.
Кінетика може бути виміряна з графіка поглинання при одній довжині хвилі протягом часу. На фіг.2 показаний графік залежності поглинання синього барвника (при 630 нм) при його реагуванні з відбілювачем.
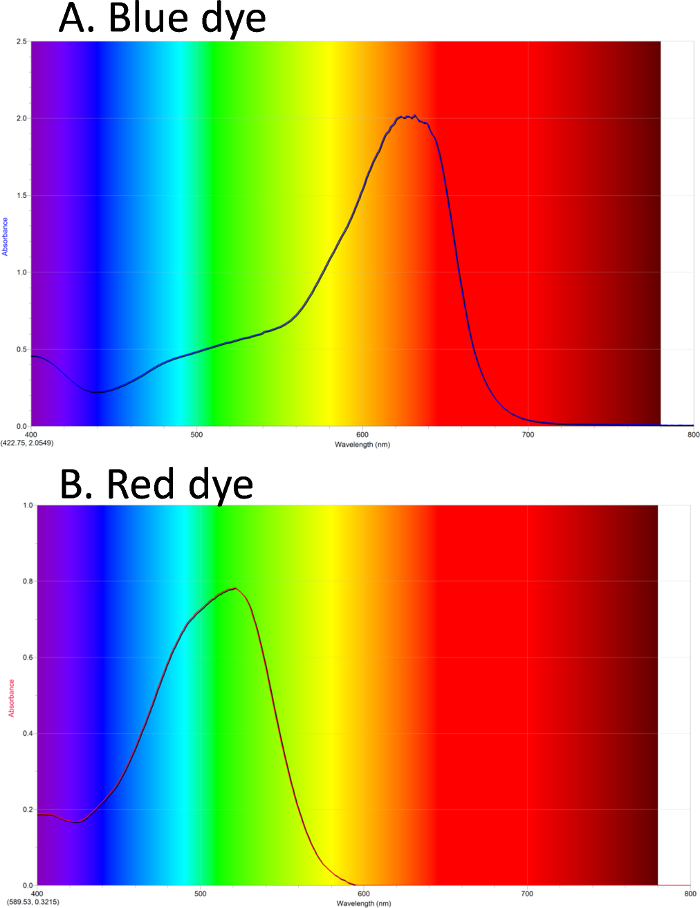
1. Спектри поглинання UV-Vis. A. Синій барвник №1 має максимальну абсорбцію в оранжевому / червоному. B. Червона фарба # 40 має максимальну абсорбцію в зеленому кольорі. Натисніть тут, щоб переглянути більшу версію цієї цифри.
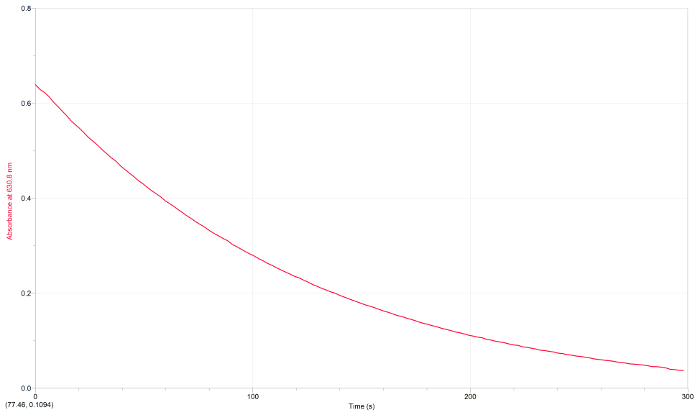
Рисунок 2. UV-Vis для кінетики. Поглинання блакитного барвника # 1 при його реагуванні з відбілювачем. Крива може підходити з експоненціальним розпадом, що вказує на кінетику першого порядку. Натисніть тут, щоб переглянути більшу версію цієї цифри.
Програми та резюме
UV-Vis використовується у багатьох хімічних аналізах. Він використовується для кількісного визначення кількості білка в розчині, оскільки більшість білків сильно поглинають при 280 нм. На фіг.3 показаний приклад спектрів цитохрому С, який має високу абсорбцію при 280 і також при 450 з-за гемової групи. UV-Vis також використовується як стандартна методика для кількісної оцінки кількості ДНК у зразку, оскільки всі підстави поглинають сильно при 260 нм. РНК і білки також поглинають при 260 нм, тому поглинання на інших довжинах хвиль можна виміряти, щоб перевірити наявність перешкод. Зокрема, білки поглинають сильно при 280 нм, так що співвідношення абсорбції при 280/260 може дати показник відношення білка до ДНК у зразку.
Найбільш прості аналізи вимірюють поглинання однієї довжини хвилі за один раз. Однак, більше хімічної інформації присутній, якщо вимірювання проводяться на багатьох довжинах хвиль одночасно. Діод-масив інструментів захопити все світло, яке передається, розділити світло на різні кольори за допомогою призми або голографічної решітки, а потім поглинання на різних довжинах хвиль захоплюється на лінійному масиві фотодіодів. Перевагою цього методу є те, що він корисний для вимірювання різних молекул одночасно.
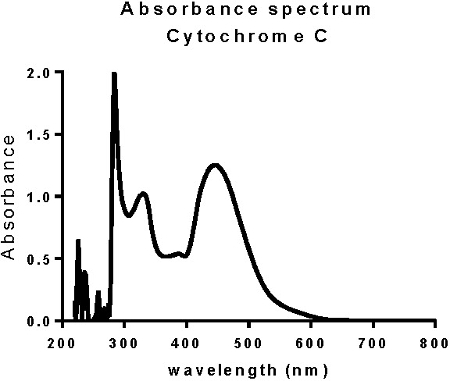
Фігура 3. УФ-віс спектр білка. Пік при 280 нм є показником білка. Пік при 450 обумовлений поглинанням гемової групи в цитохромі С.
1. Калібруйте спектрометр
- Увімкніть UV-Vis спектрометр і дайте лампам прогрітися протягом відповідного періоду часу (близько 20 хв), щоб стабілізувати їх.
- Наповніть кювету розчинником для зразка та переконайтеся, що зовні чиста. Це буде служити заготовкою і допомагає врахувати втрати світла внаслідок розсіювання або поглинання розчинником.
- Помістіть кювету в спектрометр. Переконайтеся, що кювету вирівняно належним чином, оскільки часто кювета має дві сторони, які призначені для обробки (можуть бути рифлені) і не призначені для освітлення світла.
- Зробіть читання для порожнього. Абсорбція повинна бути мінімальною, але будь-яку абсорбцію слід відняти з майбутніх зразків. Деякі інструменти можуть зберігати порожні дані і автоматично виконувати віднімання.
2. Виконайте спектр поглинання
- Наповніть кювету зразком. Щоб переконатися, що перенесення є кількісним, двічі промийте кювету зразком, а потім заповніть його близько ¾ повної. Переконайтеся, що зовні чисті відбитки пальців і т.д.
- Помістіть кювету в спектрометрі в правильному напрямку.
- Накрийте кювету, щоб запобігти впливу навколишнього світла.
- Збирають спектр поглинання, дозволяючи приладу сканувати через різні довжини хвиль і збирати поглинання. Діапазон довжин хвиль може бути встановлений з інформацією про конкретний зразок, але діапазон 200–800 нм є стандартним. Діодний масив може збирати весь спектр поглинання за один прогон.
- З зібраного спектру абсорбції визначають максимум поглинання (λmax). Повторіть збірку спектрів, щоб отримати оцінку похибки в λmax.
- Щоб скласти калібрувальну криву, збирайте спектр УФ-Віс різних зразків концентрації. Спектрометри часто обмежені в лінійному діапазоні і не можуть вимірювати величину поглинання більше 1,5. Якщо значення абсорбції для зразка знаходяться поза лінійного діапазону приладу, розбавляйте зразок, щоб отримати значення в межах лінійного діапазону.
3. Кінетичні експерименти з УФ-спектроскопією
- UV-Vis може бути використаний для експериментів з кінетики шляхом вивчення зміни абсорбції з плином часу. Для експерименту з кінетикою беруть початкове зчитування зразка.
- Швидко додайте реагент для початку хімічної реакції.
- Добре перемішують, щоб змішатися з зразком. Якщо додати невелику кількість, це можна зробити в кюветі. Альтернативно, змішати реагент з зразком і швидко влити в кювету для вимірювання.
- Вимірюють поглинання при λmax для аналіту, що представляє інтерес, протягом часу. Якщо використання реагенту вимірюється ( тобто поглинання зростає, тому що реагент менше абсорбується), то розпад покаже порядок реакції.
- Використовуючи калібрувальну криву, зробіть графік концентрації аналіту проти часу, перетворюючи значення абсорбції в концентрацію. Звідси цей графік може бути придатним до відповідних рівнянь для визначення констант швидкості реакції.
Ультрафіолетові видимі, або UV-Vis, спектроскопія є однією з найбільш популярних аналітичних методів в лабораторії.
У УФ-Vis спектроскопії світло пропускається через зразок при певній довжині хвилі в УФ або видимому спектрі. Якщо зразок поглинає частину світла, не весь світ буде проходити або передаватися. Передача - це відношення інтенсивності прохідного світла до падаючого світла і корелює з поглинанням. Абсорбцію можна використовувати кількісно, щоб отримати концентрацію зразка. Він також може бути використаний якісно, щоб ідентифікувати з'єднання шляхом зіставлення виміряної поглинання в діапазоні довжин хвиль, званих спектром абсорбції, з опублікованими даними. Це відео введе спектроскопію УФ-ВІС і продемонструє його використання в лабораторії при визначенні концентрації зразків і кінетики реакції.
Коли фотон потрапляє в молекулу і поглинається, молекула просувається з її основного стану в більш високий енергетичний стан. Різниця енергії між цими двома полями є зазором. Для того, щоб фотон поглинався, енергія фотона повинна точно збігатися з забороненою зоною. Хімічна структура визначає ширину забороненої зони; тому кожна молекула має унікальні спектри абсорбції.
Абсорбція слідує Закону Беера, що свідчить про абсорбцію, що дорівнює коефіцієнту молярного ослаблення, що перевищує довжину шляху та концентрацію. Коефіцієнт молярного ослаблення пов'язаний зі здатністю окремої сполуки поглинати світло певної довжини хвилі. Довжина шляху відноситься до відстані, пройденої світлом через зразок, що зазвичай становить 1 см для стандартних кювет. Закон Біра можна використовувати для розрахунку концентрації зразка, якщо відома абсорбція, або може бути використана калібрувальна крива.
UV-Vis часто називають загальною технікою, оскільки більшість молекул поглинають світло в діапазоні довжини хвилі, що видно з УФ. УФ-спектр простягається від 100–400 нм, а видимий спектр - від 400 до 700 нм. Однак більшість спектрофотометрів не працюють у глибині УФ-діапазону 100–200 нм, оскільки джерела світла в цьому діапазоні коштують дорого. Більшість UV-Vis спектрофотометрів використовують дейтерієву лампу для УФ-діапазону, яка виробляє світло від 170–375 нм, і лампу вольфрамової нитки для видимого діапазону, яка виробляє світло від 350-2500 нм.
Оскільки джерело світла зазвичай є лампою з широкими діапазонами довжин хвиль, то специфічна довжина хвилі абсорбції вибирається за допомогою фільтрів або монохроматора. Монохроматор - це пристрій, який просторово розділяє довжини хвиль світла, а потім розміщує вихідну щілину, де потрібна довжина хвилі світла. Монохроматор можна сканувати в діапазоні довжин хвиль, щоб забезпечити весь спектр поглинання. Це робить техніку корисною для кількісного визначення та ідентифікації широкого спектру молекул.
Тепер, коли були викладені основи УФ-Vis спектроскопії, давайте розглянемо простий ультрафіолетовий експеримент у лабораторії.
Перш ніж почати вимірювання, ввімкніть спектрофотометр і дайте лампам прогрітися протягом відповідного періоду часу, щоб стабілізувати їх.
Приготуйте заготовку, заповнивши чисту кювету розчинником зразка, а потім протріть її зовні безворсовою папером, щоб видалити відбитки пальців.
Переконайтеся, що кювети вирівняні належним чином з будь-якою виїмкою зі сторони пучка, і вставте її в спектрофотометр. Закріпіть кришку, щоб запобігти потрапленню навколишнього світла в систему.
Вимірюють поглинання заготовки на одній довжині хвилі або в діапазоні довжин хвиль. Записують або зберігають абсорбцію, так як вона повинна відніматися від поглинання зразка.
Далі відкидають заготовку і двічі промивають кювету зразком. Потім заповнюють кювету близько ¾ повної зразка. Знову протріть кювету, щоб переконатися, що вона чиста і без відбитків пальців.
Помістіть кювету в спектрофотометрі в правильній орієнтації і зафіксуйте кришку.
Збирають вимірювання поглинання або спектр на тій же довжині хвилі або діапазоні довжин хвиль, що і заготовка. Відніміть порожній спектр або вимірювання, якщо прилад не робить це автоматично.
З зібраного спектру абсорбції визначають максимум поглинання, або λmax.
Для кількісної оцінки кількості аналіту в зразку створюють калібрувальну криву, використовуючи діапазон відомих концентрацій аналіту. Для отримання додаткової інформації про те, як побудувати та використати калібрувальну криву, перегляньте відео з цієї колекції "Криві калібрування".
Вимірювання поглинання можна також використовувати для розрахунку кінетики реакції шляхом вимірювання збільшення або зменшення концентрації сполук протягом усього процесу. Починають з початкового зчитування зразка, синього барвника в цьому випадку, на максимумі абсорбції перед реакцією.
Далі швидко додають реагент, відбілювач в цьому випадку, щоб почати хімічну реакцію. Добре перемішайте, щоб він змішувався з зразком.
Вимірюють абсорбцію на максимумі поглинання протягом часу.
Показано початковий спектр абсорбції зразка синього барвника. Кольори тла показують кольори світла у видимому спектрі. Синій барвник має максимум поглинання близько 630 нм.
Кінетику реакції між синім барвником і відбілювачем вимірювали протягом часу. Абсорбція синього барвника з часом зменшується, оскільки вона реагує з відбілювачем. Абсорбція досягає близько нуля через 300 с, що вказує на те, що реакція наближається до завершення. Для отримання додаткової інформації про кінетику та реакції, будь ласка, дивіться відео JoVE Science Education "Закони про швидкість реакції".
UV-Vis спектроскопія використовується в багатьох різних областях досліджень для ідентифікації або кількісної оцінки зразка.
Наприклад, УФ-Vis спектроскопія використовується в значній мірі в біологічних полях для кількісної оцінки кількості білка в зразку. Бредфорд-аналіз часто використовується для кількісного визначення білків за допомогою барвника. Спочатку готують калібрувальну криву відомих концентрацій білка, зазвичай з використанням альбуміну бичачої сироватки або BSA. Потім до кожної зі стандартів і до зразка додають Кумасси синю забарвлення. Потім поглинання комплексу білок-барвник вимірюють при 595 нм.
Альтернативно, білки можуть бути виміряні безпосередньо за їх абсорбції при 280 нм. У цьому прикладі концентрацію білка визначають кількісно, використовуючи спектрофотометр ультранизького об'єму. Для багатьох білків абсорбція 1 корелює з концентрацією 1 мг / мл.
Ультрафіолетова спектроскопія також використовується для кількісної оцінки кількості бактеріальних клітин в культурі клітин. Для цього вимірювання поглинання або оптична щільність вимірюють при 600 нм. Як правило, вимірювання OD600 1 вказує на присутність 8 × 108 бактеріальних клітин на мл. Вимірювання щільності клітин протягом росту культури дозволяє визначити криву бактеріального росту і може допомогти визначити, коли культура знаходиться в експонентній фазі росту.
Оксид азоту та діоксид азоту, або NOx, є побічним продуктом вихлопу автомобіля і може бути шкідливим для навколишнього середовища, оскільки він утворює пошкоджуючий тропосферний озон. NOx можна виміряти шляхом взаємодії його з розчином сульфаниловой кислоти і нафтилэтилендиамина. Отриманий розчин являє собою молекулу азо-барвника рожевого кольору, інтенсивність якої прямо корелює з концентрацією NOx. Цю концентрацію можна потім визначити, використовуючи спектрофотометр UV-Vis.
Ви тільки що спостерігали за введенням JoVE в УФ-видиму спектроскопію. Тепер ви повинні зрозуміти основи роботи UV-Vis, як виміряти зразок, використовуючи UV-Vis, і як співвідносити абсорбцію з концентрацією зразка.
Дякую за перегляд!
 Наш ассоциированный член www.Bikinika.com.ua. Добро пожаловать в мир азарта и удачи! Новый сайт "Buddy.Bet" готов предоставить вам широкий выбор азартных развлечений.
Наш ассоциированный член www.Bikinika.com.ua. Добро пожаловать в мир азарта и удачи! Новый сайт "Buddy.Bet" готов предоставить вам широкий выбор азартных развлечений.